1.
质量守恒定律是自然界的基本定律之一,化学兴趣小组以“探究质量守恒定律”为主题开展实验探究。
【提出问题】化学反应前后各物质的质量总和是否相等?
【猜想与假设】猜想1:不相等;猜想2:相等。
【资料信息】碳酸钠与稀盐酸反应的化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑。
【实验探究】甲、乙两组同学用托盘天平分别称量反应前后装置的质量。
实验方案 | 方案一 | 方案二 |
实验装置 |
|
|
实验过程 | 分别将反应物及反应容器放在托盘天平上用砝码平衡 | |
取下烧杯,将铁钉浸到硫酸铜溶液中,观察到产生色固体、溶液由蓝色逐渐变为色;再将其放回托盘天平,天平的指针(填“向左”或“向右”或“不”)偏转。 | 取下烧杯并将其倾斜,使小试管中的盐酸进入烧杯中,充分反应后再放回托盘天平,天平的指针(填“向左”或“向右”或“不”)偏转。 | |
【反思评价】请讨论分析导致方案二实验结果的原因。
【得出结论】同学们经过讨论分析,得出猜想二正确。最终得出结论:的各物质的质量总和等于反应后生成的各物质的质量总和。
【解释应用】请从微观角度解释质量守恒定律:。
【总结交流】通过以上实验,在反应物不变的前提下,要使天平平衡,对方案二的改进措施是。
【拓展延伸】小华同学设计了如图实验来验证质量守恒定律,小刚同学认为该实验设计是不正确的,原因是。

【考点】
验证质量守恒定律;




 B
B 
 D
D 
















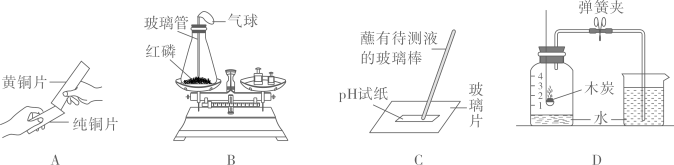
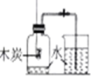 测定空气中氧气的含量
测定空气中氧气的含量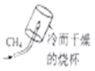 探究甲烷中是否含碳元素
探究甲烷中是否含碳元素 验证质量守恒定律
验证质量守恒定律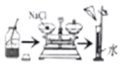 配制一定溶质质量分数的氯化钠溶液
配制一定溶质质量分数的氯化钠溶液