1.
质量守恒定律的发现,凝聚了许多科学家的心血。
材料一:早在17世纪,英国化学家波义耳在一个密闭容器中加热金属,得到了金属灰,然后打开容器盖,再次称量金属灰的质量,发现金属灰的质量比反应前的金属质量大。
材料二: 1756 年,俄国化学家洛蒙诺索夫在一个密闭的容器中加热金属锡,生成了白色的氧化锡,但容器和容器里的物质的总质量,在燃烧前后并没有发生变化。于是他认为在化学变化中物质的质量是守恒的,因此提出了质量守恒假说。
材料三: 1774 年,拉瓦锡用精确的定量实验在密封容器中研究氧化汞的分解与生成中各物质的质量之间的关系,再次对该假设加以论证。
请回答以下问题:
(1)拉瓦锡的实验证实了洛蒙诺索夫的假说,小明认为波义耳实验否定了该假说,你是否赞同小明的观点,请说明理由。
(2)小明建构了以下模型来从微观角度分析质量守恒定律,请你补充完整 。

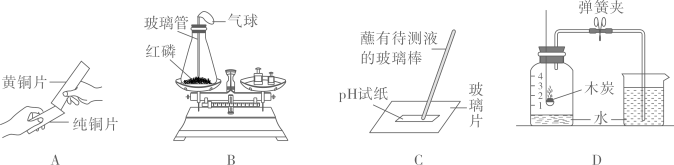
(3)为了进一步证实质量守恒定律,小明设计了如下四种实验方案,你觉得可行的是 (可多选)
A  B
B 
C  D
D 
【考点】
验证质量守恒定律;





















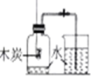 测定空气中氧气的含量
测定空气中氧气的含量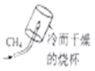 探究甲烷中是否含碳元素
探究甲烷中是否含碳元素 验证质量守恒定律
验证质量守恒定律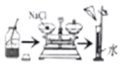 配制一定溶质质量分数的氯化钠溶液
配制一定溶质质量分数的氯化钠溶液