1.
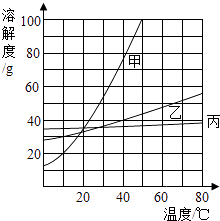
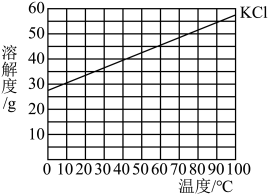
KCl在医药上可作电解质紊乱的调节剂。KCl的溶解度曲线如下图。25 ℃时,按下表数据配制溶液。下列说法不正确的是( )
序号 | ① | ② | ③ | ④ |
KCl的质量/g | 10 | 20 | 30 | 40 |
水的质量/g | 100 | 100 | 100 | 100 |
A.
KCl的溶解度随温度升高而增大
B.
①中溶质与溶液的质量比为1:11
C.
将③中溶液升温至40℃,溶液中溶质质量增大
D.
将②中溶液倒出一半,剩余溶液的溶质质量分数不变
【考点】
饱和溶液和不饱和溶液;
溶解度的影响因素;
固体溶解度曲线及其作用;
基础巩固
能力提升
变式训练
拓展培优
真题演练