1.
回答下列问题:
(1)
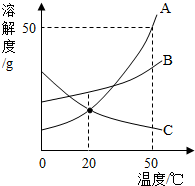
根据所给氯化钠和碳酸钠的溶解度及溶解度曲线的信息,回答下列问题:
(2)
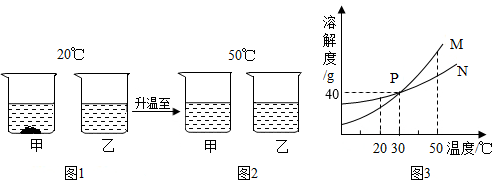
小明同学配制100g10%的氯化钠溶液,整个操作过程如图所示。
(3)
气体的溶解度也有一定的变化规律。

温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
氯化钠溶解度/g | 35 | 35.5 | 36 | 36.5 | 37 |
碳酸钠溶解度/g | 6 | 10 | 18 | 36.5 | 50 |
①t1℃时,NaCl的溶解度是g。该温度时,二者(填“能”或“不能”)形成溶质质量分数相同的饱和溶液。
②t2℃时,将40gNa2CO3固体加入50g水中,充分溶解后所得Na2CO3溶液中溶质与溶剂的质量比为。
③在不改变溶质质量分数的前提下,要使接近饱和的Na2CO3溶液变为饱和溶液,可采取的措施是。

①图中操作错误的是(填序号)。
②配制溶液的正确操作顺序为(填序号)。
③经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是(填序号)。
A.氯化钠固体不纯 B.用生锈的砝码称量
C.装瓶时有少量溶液洒出 D.溶解时烧杯内壁有水珠
④若要将100g10%的氯化钠溶液稀释成2%的溶液,需要另入水的质量为g。
①打开可乐瓶,溢出大量气体,由此可见,压强越小,CO2的溶解度越。
②不同温度下,氧气的溶解度随压强的变化如图所示,图中t1对应的温度40℃,则t2对应的温度范围是。

【考点】
饱和溶液和不饱和溶液;
溶解度的影响因素;
固体溶解度曲线及其作用;
溶质的质量分数及相关计算;
一定溶质质量分数的溶液的配制;
能力提升