1.
同学们设计了以下实验方案,以测定空气中氧气的含量。请根据下列提示,补全实验内容:

实验方法:图1所示装置可用于测定空气中氧气的含量,图2为测得实验过程中集气瓶内气体压强与时间的关系图(p0是集气瓶内初始气体压强)。
(1)实验原理:(用符号表达式表示)。
(2)实验现象:图1中冷却至室温打开止水夹后的现象为。
(3)实验结论:。
【问题与交流】
(4)①集气瓶中气体压强瞬间变大的原因是。
②该实验成功的关键是(写一点)。
【考点】
测定空气中的氧气含量;
基础巩固
能力提升
变式训练
拓展培优
真题演练

















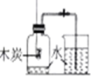 测定空气中氧气的含量
测定空气中氧气的含量 探究甲烷中是否含碳元素
探究甲烷中是否含碳元素 验证质量守恒定律
验证质量守恒定律 配制一定溶质质量分数的氯化钠溶液
配制一定溶质质量分数的氯化钠溶液