1.
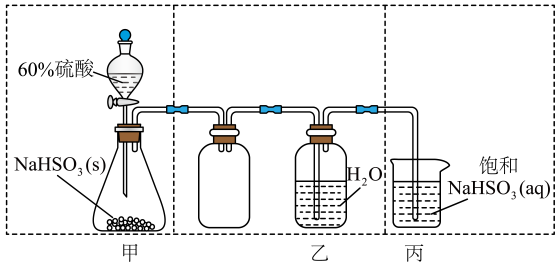
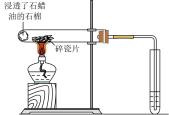
下列实验设计或实验现象正确的是
|
|
A.制备少量乙酸乙酯 | B.观察 |
|
|
C.证明 | D.收集 |
A.
A
B.
B
C.
C
D.
D
【考点】
性质实验方案的设计;
基础巩固
能力提升
变式训练
拓展培优
真题演练




 )。下列对实验现象的描述错误的是
)。下列对实验现象的描述错误的是