1.
如图所示装置常用于实验室制取常见气体。

实验一:用氯酸钾固体制取氧气
(1)仪器①的名称为。
(2)该反应的化学方程式为。
实验二:用打磨后的铝片与质量分数为2%的稀盐酸制取并收集氢气
(3)该实验可选用的装置组合是。 填字母
填字母
(4)如图所示的测得容器内气体压强与时间的关系曲线图。

①AB段气体压力变化不明显的原因是;CD段气体压力逐渐下降的原因是。
②从BC段看反应的速率是先变快后变慢,导致变慢的因素有(填序号)
a.铝片的表面积 b.盐酸的浓度 c.温度
【考点】
氧气的实验室制法;
金属的化学性质;













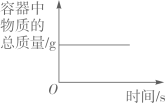 在密闭的容器中加热汞得到氧化汞
在密闭的容器中加热汞得到氧化汞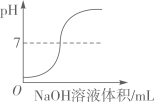 向一定量的稀盐酸中滴加氢氧化钠溶液
向一定量的稀盐酸中滴加氢氧化钠溶液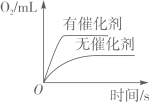 两份等质量、等溶质的质量分数的过氧化氢溶液分别制取氧气
两份等质量、等溶质的质量分数的过氧化氢溶液分别制取氧气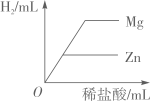 向等质量的Zn和Mg中分别滴加等溶质质量分数的稀盐酸
向等质量的Zn和Mg中分别滴加等溶质质量分数的稀盐酸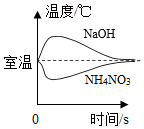 把NaOH和NH4NO3固体分别溶于水中
把NaOH和NH4NO3固体分别溶于水中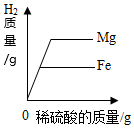 分别向等质量镁和铁中,逐渐加入溶质质量分数相同的稀硫酸至过量
分别向等质量镁和铁中,逐渐加入溶质质量分数相同的稀硫酸至过量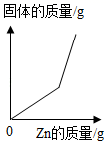 向一定质量硝酸银的混合溶液中逐渐加入锌粉
向一定质量硝酸银的混合溶液中逐渐加入锌粉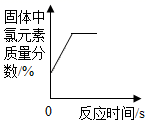 加热一定质量氯酸钾和二氧化锰的固体混合物
加热一定质量氯酸钾和二氧化锰的固体混合物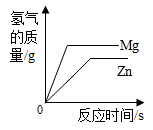 向两份等质量,相同质量分数的稀硫酸中,分别不断加入镁粉和锌粉
向两份等质量,相同质量分数的稀硫酸中,分别不断加入镁粉和锌粉 向一定质量二氧化锰固体中加入一定质量的过氧化氢溶液
向一定质量二氧化锰固体中加入一定质量的过氧化氢溶液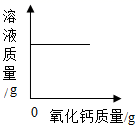 温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙
温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙 向一定质量硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液。
向一定质量硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液。