1.
下列各组变化中,每一转化在一定条件下均能一步实现的是

A.
只有②
B.
①和②
C.
②③
D.
①和③
【考点】
氧气的实验室制法;
金属的化学性质;
 注意明火
注意明火 小心用电
小心用电 小心烫伤
小心烫伤 实验后洗手
实验后洗手











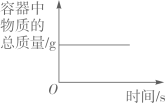 在密闭的容器中加热汞得到氧化汞
在密闭的容器中加热汞得到氧化汞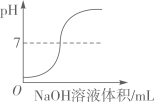 向一定量的稀盐酸中滴加氢氧化钠溶液
向一定量的稀盐酸中滴加氢氧化钠溶液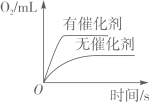 两份等质量、等溶质的质量分数的过氧化氢溶液分别制取氧气
两份等质量、等溶质的质量分数的过氧化氢溶液分别制取氧气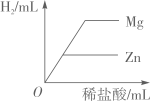 向等质量的Zn和Mg中分别滴加等溶质质量分数的稀盐酸
向等质量的Zn和Mg中分别滴加等溶质质量分数的稀盐酸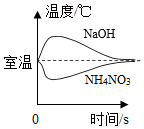 把NaOH和NH4NO3固体分别溶于水中
把NaOH和NH4NO3固体分别溶于水中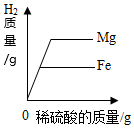 分别向等质量镁和铁中,逐渐加入溶质质量分数相同的稀硫酸至过量
分别向等质量镁和铁中,逐渐加入溶质质量分数相同的稀硫酸至过量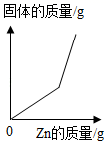 向一定质量硝酸银的混合溶液中逐渐加入锌粉
向一定质量硝酸银的混合溶液中逐渐加入锌粉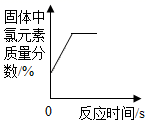 加热一定质量氯酸钾和二氧化锰的固体混合物
加热一定质量氯酸钾和二氧化锰的固体混合物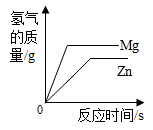 向两份等质量,相同质量分数的稀硫酸中,分别不断加入镁粉和锌粉
向两份等质量,相同质量分数的稀硫酸中,分别不断加入镁粉和锌粉 向一定质量二氧化锰固体中加入一定质量的过氧化氢溶液
向一定质量二氧化锰固体中加入一定质量的过氧化氢溶液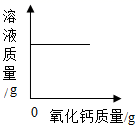 温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙
温度不变,向一定质量饱和氢氧化钙溶液中加入氧化钙 向一定质量硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液。
向一定质量硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液。