1.
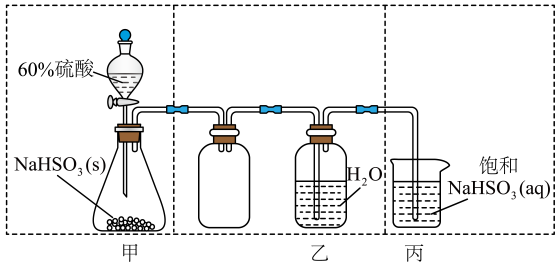
对硝基苯甲酸广泛应用于医药、染料、感光材料等领域。实验室用下图示装置制备(加热和夹持仪器已略去)。反应原理为:


 。
。

实验步骤:
I.向三口烧瓶中加入
水,再加入微量的溴化四丁基铵(结构如图)。加热待温度达到
, 恒温分批共加入
对硝基甲苯。升温到一定温度控制条件反应。

溴化四丁基铵
Ⅱ.反应结束后趁热过滤,洗涤固体,合并洗涤液。
Ⅲ.向滤液中加入 , 调节
至
, 析出黄白色沉淀。待沉淀完全后,过滤,洗涤。经过重结晶,得到对硝基苯甲酸
。
熔点 | 沸点 | 溶解性 | |
对硝基甲苯 | 51.3 | 238(易升华) | 不溶于水,溶于乙醇 |
对硝基苯甲酸 | 242 | - | 微溶于水,溶于乙醇 |
回答下列问题:
(1)
仪器a的名称是。
(2)
根据下列实验数据,从经济环保的角度选择的温度条件和时间分别是,加热方式为。温度过高会造成产率下降,可能原因是。
(3)
步骤Ⅱ反应结束后趁热过滤除去(填化学式),用洗涤固体并合并滤液。
(4)
溴化四丁基铵有类似冠醚的作用(吸引 )。解释溴化四丁基铵在该实验中的作用。
(5)
计算对硝基苯甲酸的产率(保留2位有效数字)。
)。解释溴化四丁基铵在该实验中的作用。
(5)
计算对硝基苯甲酸的产率(保留2位有效数字)。

【考点】
制备实验方案的设计;
能力提升
真题演练