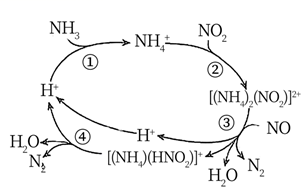
1.
高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。

|
|
|
|
|
|
开始沉淀pH |
1.9 |
4.2 |
6.2 |
|
沉淀完全pH |
3.2 |
6.7 |
8.2 |
下列说法错误的是( )
A.
固体X主要成分是 和S;金属M为Zn
B.
浸取时,增大
和S;金属M为Zn
B.
浸取时,增大 压强可促进金属离子浸出
C.
中和调pH的范围为3.2~4.2
D.
还原时,增大溶液酸度有利于Cu的生成
压强可促进金属离子浸出
C.
中和调pH的范围为3.2~4.2
D.
还原时,增大溶液酸度有利于Cu的生成
【考点】
氧化还原反应;
制备实验方案的设计;