1.
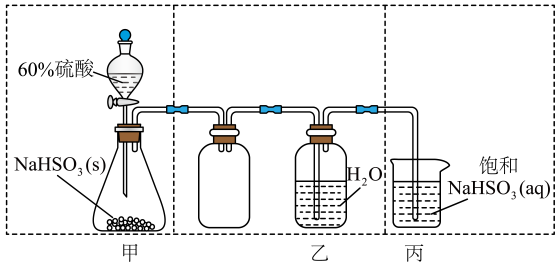
氮化铬( )是一种耐磨性良好的新型材料,难溶于水。探究小组同学用下图所示装置(夹持装置略去)在实验室中制取氮化铬并测定所得氮化铬的纯度。
)是一种耐磨性良好的新型材料,难溶于水。探究小组同学用下图所示装置(夹持装置略去)在实验室中制取氮化铬并测定所得氮化铬的纯度。

已知:实验室中常用溶液与
溶液反应制取
;
易潮解,高温下易被氧气氧化;
中发生反应:
。
回答下列问题:
(1)
实验中 的作用是;制取
的作用是;制取 的化学反应方程式为。
(2)
试剂
的化学反应方程式为。
(2)
试剂 的名称是。
(3)
盛放饱和
的名称是。
(3)
盛放饱和 溶液的仪器叫“恒压滴液漏斗”,与普通分液漏斗相比,使用该仪器的好处是。
(4)
实验过程中需间歇性微热
溶液的仪器叫“恒压滴液漏斗”,与普通分液漏斗相比,使用该仪器的好处是。
(4)
实验过程中需间歇性微热 处导管的目的是。
(5)
向
处导管的目的是。
(5)
向 所得
所得 中加入足量
中加入足量 溶液,然后通入水蒸气将
溶液,然后通入水蒸气将 全部蒸出,将
全部蒸出,将 用
用 溶液完全吸收,则所得产品中
溶液完全吸收,则所得产品中 的质量分数为(保留三位有效数字)。
的质量分数为(保留三位有效数字)。
【考点】
制备实验方案的设计;
能力提升
真题演练


 b.
b.
 d.
d.