1.
硫酰氯( )是化工生产的重要原料,实验室制备
)是化工生产的重要原料,实验室制备 的原理为
的原理为 , 该反应会放出大量的热。已知:
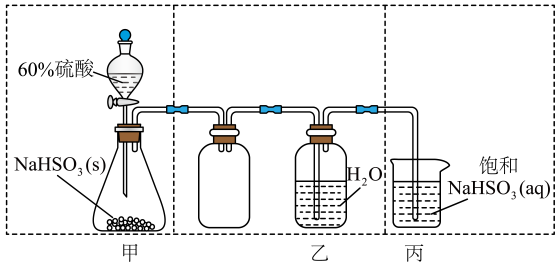
, 该反应会放出大量的热。已知: 的熔点为-54.1℃,沸点为69.1℃,能与水发生剧烈反应产生白雾。其实验装置如图所示(部分夹持仪器已省略),请回答下列问题:
的熔点为-54.1℃,沸点为69.1℃,能与水发生剧烈反应产生白雾。其实验装置如图所示(部分夹持仪器已省略),请回答下列问题:

(1)
若使用Cu与浓硫酸反应制备 , 请写出该反应的化学方程式:,与之匹配的装置图为(填“I”或“Ⅱ”),该反应体现了浓硫酸的性。
(2)
装置乙中仪器B的名称为,不能盛放
, 请写出该反应的化学方程式:,与之匹配的装置图为(填“I”或“Ⅱ”),该反应体现了浓硫酸的性。
(2)
装置乙中仪器B的名称为,不能盛放 的理由是。
(3)
若无装置甲与装置丙,制得的
的理由是。
(3)
若无装置甲与装置丙,制得的 中会混有(填化学式)。
(4)
若将乙中的尾气通入品红溶液中,品红溶液褪色,某课外小组的同学对品红溶液褪色的原因提出猜想:
(5)
为测定空气中
中会混有(填化学式)。
(4)
若将乙中的尾气通入品红溶液中,品红溶液褪色,某课外小组的同学对品红溶液褪色的原因提出猜想:
(5)
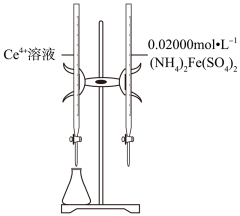
为测定空气中 的含量,该课外小组的同学将空气样品通200mL
的含量,该课外小组的同学将空气样品通200mL 的酸性
的酸性 溶液。若通入的空气为VmL,溶液恰好褪色,假定样品中的
溶液。若通入的空气为VmL,溶液恰好褪色,假定样品中的 可被溶液充分吸收,则该空气样品中
可被溶液充分吸收,则该空气样品中 的含量是
的含量是 。
。

a.使品红溶液褪色
b.与
生成的HClO使品红溶液褪色
c.两者共同作用使品红溶液褪色
①设计实验检验猜想a是否正确:。
②甲同学认为向氯水中通入一定量的可增强其漂白性,乙同学认为该观点错误,原因是(用离子方程式表示)。
【考点】
制备实验方案的设计;
能力提升
真题演练



 b.
b.
 d.
d.