1.
对比实验是实验探究的重要方法,下列对比实验设计能实现相应实验目的的是( )
选项 | 实验目的 | 实验设计 | 选项 | 实验目的 | 实验设计 |
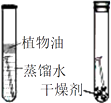
A | 探究温度对分子运动快慢的影响 |
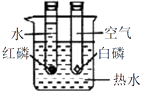
| B | 探究水对铁钉锈蚀的影响 |
|
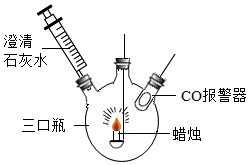
C | 探究空气是燃烧的必要条件 |
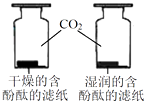
| D | 探究CO2与水反生反应 |
|
A.
A
B.
B
C.
C
D.
D
【考点】
探究二氧化碳的性质;
燃烧的条件与灭火原理探究;
探究金属锈蚀的条件;
基础巩固
能力提升
变式训练
拓展培优