1.
用下图装置进行实验。
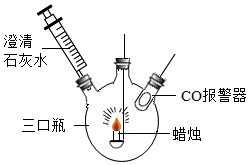
| 操作步骤 | 现象 | 原理及结论 |
| (1)将点燃的蜡烛伸入瓶中,塞紧胶塞 | 一段时间后,CO报警器发出报警声 | 蜡烛燃烧有CO生成 |
| (2)蜡烛熄灭后,冷却至室温 |
| 蜡烛燃烧有水生成 |
| (3)将澄清石灰水推入瓶中 | 澄清石灰水变浑浊 | 化学方程式为 |
| (4)实验分析:通过该实验可知,蜡烛中一定含有的元素是。 | ||
【考点】
探究二氧化碳的性质;
基础巩固
能力提升
变式训练
拓展培优
真题演练














