1.
25℃时,部分物质的电离平衡常数如表所示,请回答下列问题
化学式 | CH3COOH | NH3·H2O | H2CO3 | H2SO3 |
电离平衡常数 | 1.75×10-5 | 1.8×10-5 | K1=4.5×10-7 , K2=4.7×10-11 | K1=1×10-2 , K2=6.0×10-8 |
(1)
上述等浓度的四种溶液,导电能力最强的是,用蒸馏水稀释0.10mol/L的醋酸,下列各式表示的数值随水量的增加而增大的是(填序号)。
(2)
25℃时,NaHSO3的水解平衡常数Kh=,溶液显性。
(3)
若向氨水中加入稀硫酸至恰好中和,所得溶液的pH(填“>”“=”或“<”)7,用离子方程式表示其原因:。若向氨水中加入稀硫酸至溶液pH=7,此时溶液中的 =a mol/L,则
=a mol/L,则 mol/L。
(4)
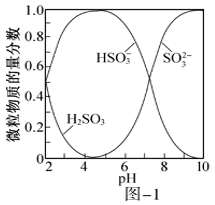
相同温度下,等pH的①CH3COONa溶液;②Na2CO3溶液;③Na2SO3溶液,三种溶液的物质的量浓度由大到小排序为。少量SO2通入Na2CO3溶液的离子方程式为。
mol/L。
(4)
相同温度下,等pH的①CH3COONa溶液;②Na2CO3溶液;③Na2SO3溶液,三种溶液的物质的量浓度由大到小排序为。少量SO2通入Na2CO3溶液的离子方程式为。
a. b.
c.
【考点】
弱电解质在水溶液中的电离平衡;
盐类水解的应用;
能力提升
真题演练