1.
目前,“污渍爆炸盐”已成为广泛应用 洗涤助剂之一。其主要成分是Na2CO3·nH2O2 , 俗称固体双氧水,溶于水生成Na2CO3和H2O2。探究小组制得“污渍爆炸盐”的饱和水溶液,向其中加入一定量澄清石灰水,产生白色沉淀,过滤得到滤液和滤渣。
洗涤助剂之一。其主要成分是Na2CO3·nH2O2 , 俗称固体双氧水,溶于水生成Na2CO3和H2O2。探究小组制得“污渍爆炸盐”的饱和水溶液,向其中加入一定量澄清石灰水,产生白色沉淀,过滤得到滤液和滤渣。
【提出问题】滤液中溶质的成分是什么?
【作出猜想】猜想一:NaOH;猜想二:NaOH、Ca(OH)2;猜想三:NaOH、Na2CO3;猜想四:NaOH、Na2CO3、Ca(OH)2
(1)
以上猜想中,有一个猜想是错误的,其原因是(用化学方程式表示)。
(2)
【实验探究】
(3)
【拓展应用】
实验步骤 | 实验现象 | 实验结论 | |
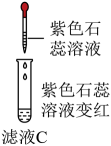
操作一 | 取少量滤液于试管中,滴加溶液 | 产生白色沉淀 | 猜想二成立 |
操作二 | 另取少量滤液于试管中,滴加过量稀盐酸 | 。 | 猜想三不成立 |
“污渍爆炸盐”除用作洗涤助剂之外,还可用作。
【反思交流】“污渍爆炸盐”应密封保存。
【考点】
盐的化学性质;
实验探究物质的组成成分以及含量;
能力提升
真题演练