1.
重外化学兴趣小组同学向硫酸镁溶液中加入氢氧化钡溶液,向氯化钡溶液中加入稀硫酸,然后过滤,将两种滤液混合,溶液中产生白色沉淀,又过滤得滤渣和滤液C如图所示:

(1)
试管A中发生反应的化学方程式为:。
(2)
【提出问题】:滤液C中含什么离子?
(3)
【探究实验2】
(4)
【实验探究3】为了最终得出滤液C中的离子成分,小灵同学另取滤液C,先加入足量氢氧化钠溶液,然后加入碳酸钠溶液,均观察到溶液中产生白色沉淀。
【探究实验1】
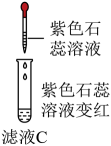
小凤同学取滤液C并加入几滴紫色石蕊溶液,如图所示,根据实验现象得出滤液C中一定含有(填离子符号),同时推得一定不含有(填离子符号)。将上图中试管A和B分别过滤得到的滤液混合后所得的白色沉淀的成分是(填化学式)。
为了得出滤液C中离子成分,小雨同学另取滤液C,加入少量的氢氧化钡溶液,如图所示,没有观察到明显的现象,由此小雨同学得出滤液C中一定不含的离子是(填离子符号)。

【总结】
根据以上三个探究,最终得出滤液C中含有的离子是。(填离子符号)
【考点】
盐的化学性质;
实验探究物质的组成成分以及含量;
能力提升
真题演练

