1.
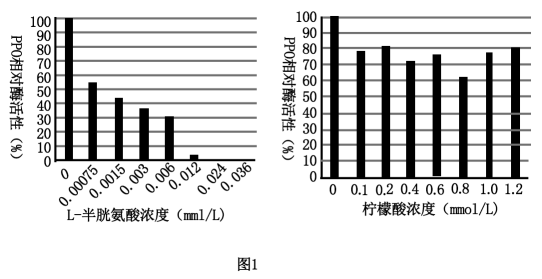
苹果汁加工过程中,苹果细胞中的多酚氧化酶(PPO)可催化酚类物质发生氧化,引起褐变反应,影响果汁的色泽和口感。已知L-半胱氨酸和柠檬酸钠是两种PPO抑制剂,科研人员研究了不同浓度的上述两种物质对PPO相对酶活性的影响,结果如图1。回答下列问题:

(1)
上述实验的自变量是。由图中结果可知,在苹果汁加工过程中,选用作为PPO抑制剂效果可能更好,理由是。
(2)
图2为酶和两种酶抑制剂的作用机理示意图。为研究L-半胱氨酸的作用机理,在酶量一定的条件下,科研人员检测了加入L-半胱氨酸对PPO酶促反应速率的影响,结果如图3。
①由图2中的A可知,底物与酶的活性部位结构互补时,酶才能发挥作用,体现酶具有性。
②据图3分析,限制a点酶促反应速率的因素是,L-半胱氨酸的作用机理为图2中的(选填“B”或“C”)。
【考点】
酶的特性;
探究影响酶活性的因素;
能力提升
真题演练