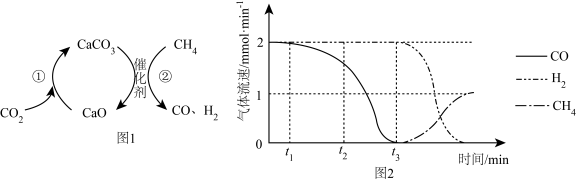
1.
下列工业生产中采用的措施与目的相符合的是( )
A.
高炉炼铁时通过加入过量铁矿石提高化学反应速率
B.
硫酸工业中用热交换器,以维持反应条件、节约能源
C.
合成氨中循环利用 、
、 , 以提高产率、降低成本
D.
海带提碘时通过浓缩提高
, 以提高产率、降低成本
D.
海带提碘时通过浓缩提高 , 以减少氧化剂的用量
, 以减少氧化剂的用量
【考点】
化学反应速率;
化学反应速率的影响因素;