1.
富马酸亚铁(结构简式为 )对胃黏膜刺激较小,是一种治疗缺铁性贫血的安全有效的铁制剂。某实验小组制备富马酸亚铁并测定产品中铁的质量分数。
)对胃黏膜刺激较小,是一种治疗缺铁性贫血的安全有效的铁制剂。某实验小组制备富马酸亚铁并测定产品中铁的质量分数。
 )对胃黏膜刺激较小,是一种治疗缺铁性贫血的安全有效的铁制剂。某实验小组制备富马酸亚铁并测定产品中铁的质量分数。
)对胃黏膜刺激较小,是一种治疗缺铁性贫血的安全有效的铁制剂。某实验小组制备富马酸亚铁并测定产品中铁的质量分数。
(1)
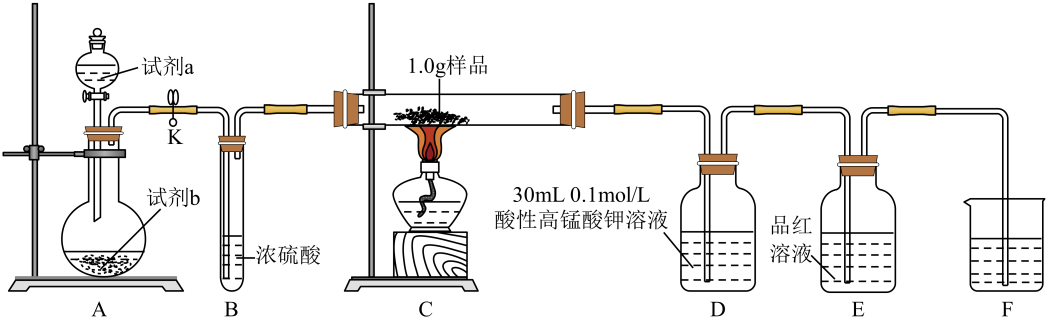
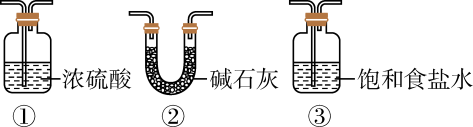
制备富马酸(实验装置如图所示,夹持装置已略去)
(2)
合成富马酸亚铁
(3)
测定产品中铁的质量分数

将NaClO3和V2O5置于三颈烧瓶中,滴加糠醛,在90~100℃条件下持续加热3~4h,制得富马酸。
①仪器A的名称是 。
②冷却液宜从(填“a”或“b”)口进入。
③实验中球形冷凝管的作用是。
①取精制后的富马酸(HOOC-CH=CH-COOH)溶于适量水中,加入碳酸钠调节pH为6.5~6.7,加热、搅拌,产生大量气泡。产生气泡的化学方程式为。
②将硫酸亚铁溶液和适量的Na2SO3溶液缓慢加入上述反应液中,维持温度为100℃并充分搅拌3~4h。加入适量的Na2SO3溶液的目的是。
③经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等得到产品。
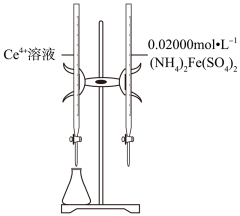
准确称取产品ag,加入新煮沸过的3mol·L-1H2SO4溶液15mL,待样品完全溶解后,再加入新煮沸过的冷水50mL和4滴邻二氮菲—亚铁指示剂,此时溶液呈红色;立即用cmol·L-1(NH4)2Ce(SO4)3标准液滴定(Ce4++Fe2+=Ce3++Fe3+ , 假设杂质不反应),滴定到终点(溶液变为浅蓝色)时消耗标准液VmL。
①(NH4)2Ce(SO4)3标准液适宜盛放在(填“酸式”或“碱式”)滴定管中。
②该实验中能否用KMnO4标准液代替(NH4)2Ce(SO4)3标准液滴定Fe2+ , 说明理由。
③产品中铁的质量分数为 (用含c、a、V的代数式表示)。
④若滴定前平视读数,终点时仰视读数会导致测量结果偏 (填“低”或“高”)。
【考点】
探究物质的组成或测量物质的含量;
能力提升
真题演练