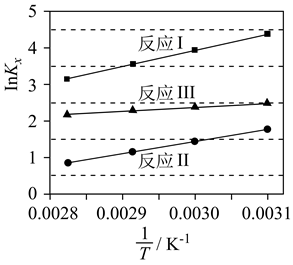
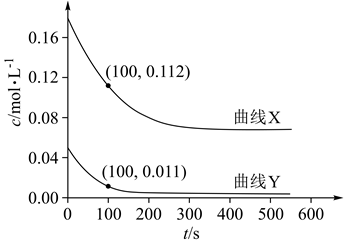
1.
我国科学家研制出催化剂将CO2转化为烃的效率提高1000倍。已知:在某催化剂作用下,CO2和H2发生反应如下:4CO2(g) +13H2(g) C4H10(g) +8H2O(g) △H
C4H10(g) +8H2O(g) △H
(1)
已知C4H10(g)、H2(g)的燃烧热△H分别为-2900 kJ·mol-1、-285.8 kJ·mol-1 , H2O(I)=H2O(g) △H3= +44 kJ·mol-1.则△H=kJ·mol-1。
(2)
在恒容恒温条件下,向密闭容器中充入CO2、H2 , 加入合适催化剂发生上述反应,下列情况表明反应达到平衡状态的是____(填字母)。
A.
混合气体密度保持不变
B.
气体总压强保持不变
C.
气体平均摩尔质量保持不变
D.
混合气体中C4H10体积分数保持不变
(3)
在密闭容器中充入适量CO2和H2 , 发生上述反应,单位时间内CO2的转化率与温度、催化剂的关系如图1所示。
(4)
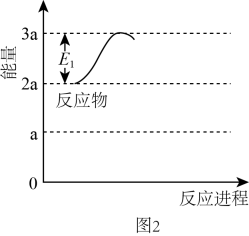
在密闭容器中充入0.4 mol CO2和1.3 mol H2发生上述反应,测得CO2的平衡转化率与温度、压强的关系如图2所示。

①催化效率,Cat2(填“>”、“<”或“=”)Catl。
②a点(填 “达到”或 “未达到”)平衡,理由是。b点之后CO2的转化率降低,可能的原因是。

①p2 (填 “>”、 “<”或 “=”)p1 , 随着温度升高,不同压强下,CO2的平衡转化率接近相等,其主要原因是。
②已知M点对应的容器体积为1 L,则在300℃下平衡常数K=(只列计算式)。
【考点】
化学平衡转化过程中的变化曲线;
化学反应速率与化学平衡的综合应用;
能力提升
真题演练






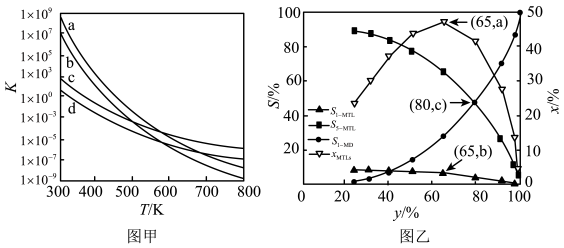
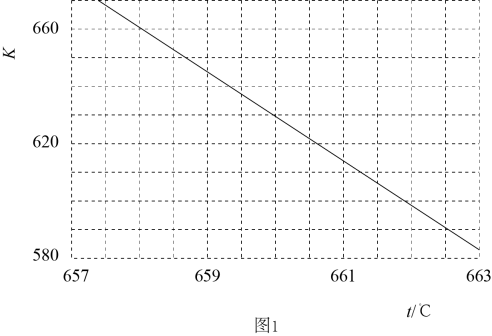
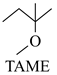 △H1
△H1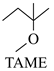 △H2
△H2