1.
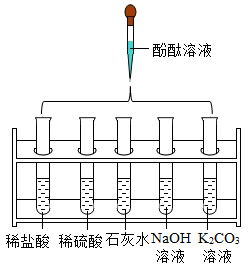
用下图装置完成实验。
|
装置 |
试剂 |
现象 |
结论 |
|
| a为NaOH溶液,b为澄清石灰水,c为无色酚酞溶液 |
| NaOH溶液和澄清石灰水均呈碱性 |
| a、b为稀盐酸或澄清石灰水c为Na2CO3溶液 | I中产生无色气体,II中出现的现象是 | 写出I中的化学反应方程式 |
【考点】
酸碱指示剂的性质及应用;
物质的鉴别、推断;
基础巩固
能力提升
变式训练
拓展培优
真题演练