1.
反应Ⅰ可用于在国际空间站中处理二氧化碳,同时伴有副反应Ⅱ发生。
主反应Ⅰ.CO2(g)+4H2(g)CH4(g)+2H2O(g) △H1=-270kJ·mol-1
副反应Ⅱ.CO2(g)+H2(g)CO(g)+H2O(g) △H2
回答下列问题:
(1)
几种化学键的键能如表所示:
(2)
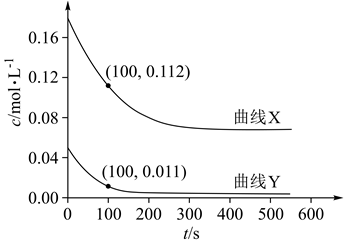
为了进一步研究上述两个反应,某小组在三个容积相同的刚性容器中,分别充入1molCO2和4molH2 , 在三种不同实验条件(见表)下进行两个反应,反应体系的总压强(p)随时间变化情况如图所示:
(3)
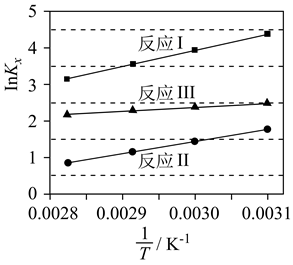
对于反应Ⅰ,在一定条件下存在:v正(H2)=k1•c4(H2)•c(CO2)或v逆(H2O)=k2•c2(H2O)•c(CH4),相应的速率与温度关系如图所示。
化学键 | C—H | H—H | H—O | C=O |
键能/kJ·mol-1 | 413 | 436 | 463 | a |
则a=。

实验编号 | a | b | c |
温度/K | T1 | T1 | T2 |
催化剂的比表面积/(m2•g-1) | 80 | 120 | 120 |
①T1T2(填“>”“<”或“=”),曲线Ⅲ对应的实验编号是。
②若在曲线Ⅱ的条件下,10min达到平衡时生成1.2molH2O,则10min内反应的平均速率v(H2O)=kPa•min-1 , 反应Ⅱ的平衡常数Kp=。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)

反应Ⅰ的平衡常数K=(用含k1 , k2的代数式表示);图中A、B、C、D四个点中,能表示反应已达到平衡状态的是。
【考点】
反应热和焓变;
化学反应速率与化学平衡的综合应用;
能力提升
真题演练





 △H1
△H1 △H2
△H2