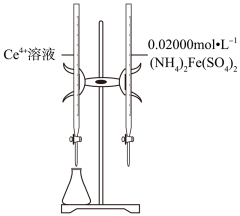
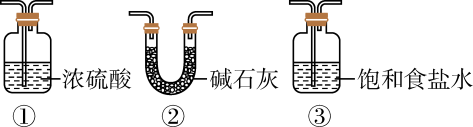
1.
以磷石膏(含CaSO4和少量SiO2、Fe2O3等)为原料制备轻质碳酸钙和铝铵矾的实验流程如图所示。

回答下列问题:
(1)
“转化”步骤中CaSO4转化成CaCO3的化学方程式为。
(2)
铝铵矾【NH4Al(SO4)2·12H2O】是一种絮凝剂。请补充由“转化”后的滤液制取铝铵矾的实验方案:
(3)
利用图2装置模拟制备轻质碳酸钙(CaCO3)
①向滤液中加入,至不再产生气体,将所得溶液经系列操作制得(NH4)2SO4固体。
②向Al2(SO4)3溶液中加入(NH4)2SO4固体,边加边搅拌,待固体完全溶解后,将所得
溶液蒸发浓缩、、过滤、洗涤、干燥,得到铝铵矾(部分物质的溶解度随温度的变化如图1所示)。
图1 图2
图2
①A中反应的化学方程式为;装置B中盛有的试剂是。
②多孔球泡的作用是;C中反应的化学方程式为。
【考点】
制备实验方案的设计;
能力提升
真题演练