1.
请回答下列问题:
(1)
对烟道气中的 进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由
进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由 和CO反应生成S和
和CO反应生成S和 的能量变化如图所示,已知每生成
的能量变化如图所示,已知每生成 , 那该反应(填“放出”或“吸收”)的热量为kJ。
(2)
, 那该反应(填“放出”或“吸收”)的热量为kJ。
(2)
 与
与 反应生成
反应生成 和一种黑色固体。在25℃、
和一种黑色固体。在25℃、 下,已知该反应每转移
下,已知该反应每转移 , 放热44.4kJ,写出该反应的热化学方程式。
(3)
近年来空气污染日益严重,原因之一是汽车尾气中含有
, 放热44.4kJ,写出该反应的热化学方程式。
(3)
近年来空气污染日益严重,原因之一是汽车尾气中含有 、
、 、
、 等气体。为消除汽车尾气的污染,可采取:NO和CO在催化转换器中发生如下反应:
(4)
工业上接触法生产硫酸的主要反应之一是:在一定的温度、压强和钒催化剂存在的条件下,
等气体。为消除汽车尾气的污染,可采取:NO和CO在催化转换器中发生如下反应:
(4)
工业上接触法生产硫酸的主要反应之一是:在一定的温度、压强和钒催化剂存在的条件下, 被空气中的
被空气中的 氧化为
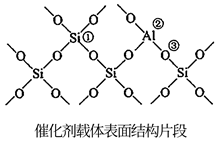
氧化为 是钢催化剂的活性成分,郭汗贤等提出:
是钢催化剂的活性成分,郭汗贤等提出: 在对反应Ⅰ的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,图示如下:
在对反应Ⅰ的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,图示如下:

;
已知:;
CO的燃烧热为;
与CO发生反应的热化学方程式:
,
(用
、
、
表示)。

有关气体分子中1mol化学键断裂时需要吸收的能量数据如下:
化学键 | |||
能量 | 535 | 496 | 472 |
①由此计算反应Ⅰ的。
②反应Ⅱ、Ⅲ的化学方程式为、。
【考点】
反应热和焓变;
盖斯定律及其应用;
能力提升
真题演练










 (g) ∆H1<0
(g) ∆H1<0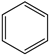 (g)+15O2(g)⇌12CO2(g)+6H2O(l) ∆H4
(g)+15O2(g)⇌12CO2(g)+6H2O(l) ∆H4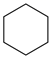 (g)+9O2(g)=6CO2(g)+6H2O(l) ∆H5
(g)+9O2(g)=6CO2(g)+6H2O(l) ∆H5