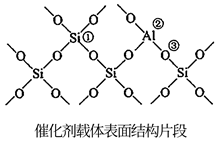
1.
能源是现代社会物质文明的原动力,研究化学反应能量变化意义重大。回答下列问题:
I.氢能是极具发展潜力的清洁能源,被誉为“21世纪终极能源”。氢气的制备和应用是目前的研究热点。
(1)
工业生产中可利用 还原
还原 制备清洁能源甲醇。
(2)
热化学硫碘循环分解水是一种有发展前景的制氢方法之一,反应过程如图:
制备清洁能源甲醇。
(2)
热化学硫碘循环分解水是一种有发展前景的制氢方法之一,反应过程如图:
①由如图的能量转化关系可知生成需要(填“吸收”或“放出”)
能量。

②已知和
的燃烧热分别为
。则
的
。

反应I:
反应II:
反应III:
①在热化学硫碘循环分解水的总反应中,反应物的总能量(填“”、“
”或“
”)生成物总能量,热化学方程式为。
②已知中
键完全断裂时需要吸收
的能量,
中
键形成时放出
的能量,则
中
键断裂时吸收的能量为
。
【考点】
反应热和焓变;
盖斯定律及其应用;
能力提升
真题演练










 (g) ∆H1<0
(g) ∆H1<0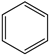 (g)+15O2(g)⇌12CO2(g)+6H2O(l) ∆H4
(g)+15O2(g)⇌12CO2(g)+6H2O(l) ∆H4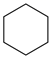 (g)+9O2(g)=6CO2(g)+6H2O(l) ∆H5
(g)+9O2(g)=6CO2(g)+6H2O(l) ∆H5