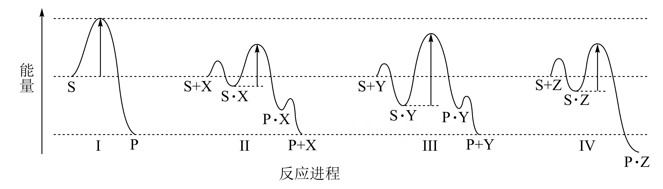
1.
下列说法或表示方法正确的是
A.
已知:500℃、30MPa下,N2(g)+3H2(g) 2NH3(g)∆H= -92.4 kJ/mol,则1.5molH2和过量的N2在此条件下充分反应。放出热量等于46.2kJ
B.
由C(s,石墨)= C(s,金刚石)∆H=+1.90kJ·mol-1 可知,金刚石比石墨稳定
C.
在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=H2O(l)∆H= -285.8kJ·mol-1
D.
在稀溶液中,H+(aq)+OH-(aq) = H2O(l)∆H= -57.3kJ·mol-1 , 若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ
2NH3(g)∆H= -92.4 kJ/mol,则1.5molH2和过量的N2在此条件下充分反应。放出热量等于46.2kJ
B.
由C(s,石墨)= C(s,金刚石)∆H=+1.90kJ·mol-1 可知,金刚石比石墨稳定
C.
在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=H2O(l)∆H= -285.8kJ·mol-1
D.
在稀溶液中,H+(aq)+OH-(aq) = H2O(l)∆H= -57.3kJ·mol-1 , 若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ
【考点】
化学反应中能量的转化;