1.
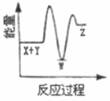
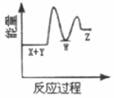
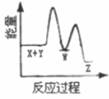
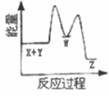
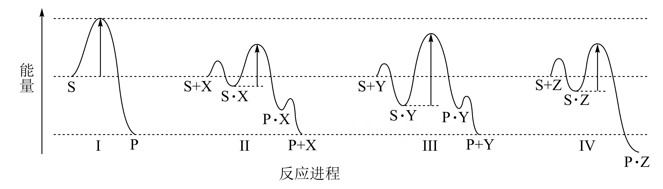
理论研究表明,在101kPa和298K下,  异构化反应过程的能量变化如图所示。下列说法错误的是( )
异构化反应过程的能量变化如图所示。下列说法错误的是( )

A.
HCN比HNC稳定
B.
该异构化反应的  C.
正反应的活化能大于逆反应的活化能
D.
使用催化剂,可以改变反应的反应热
C.
正反应的活化能大于逆反应的活化能
D.
使用催化剂,可以改变反应的反应热
【考点】
化学反应中能量的转化;