1.
50 0.50
0.50 盐酸与50
盐酸与50 0.55
0.55
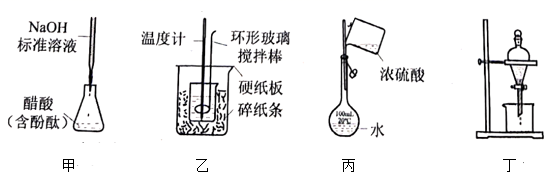
 溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热。回答下列问题:
溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热。回答下列问题:

(1)
从实验装置上看,图中尚缺少的一种玻璃仪器是。
(2)
隔热层的作用是。
(3)
倒入 溶液的正确操作是(填字母)。
(4)
若实验过程中,内筒未加杯盖,求得的中和反应反应热
溶液的正确操作是(填字母)。
(4)
若实验过程中,内筒未加杯盖,求得的中和反应反应热 (填“偏大”“偏小”或“无影响”)。
(5)
假设盐酸和氢氧化钠溶液的密度都是1
(填“偏大”“偏小”或“无影响”)。
(5)
假设盐酸和氢氧化钠溶液的密度都是1 , 又知中和反应后所得溶液的比热容
, 又知中和反应后所得溶液的比热容 。为了计算中和反应反应热,某学生的实验记录数据如下:
。为了计算中和反应反应热,某学生的实验记录数据如下:
a.沿玻璃棒缓慢倒入 b.分三次倒入 c.一次迅速倒入
实验序号 | 反应物的温度/℃ | 反应前体系的温度 | 反应后体系的温度 | |
盐酸 | 氢氧化钠溶液 | |||
1 | 20.0 | 20.1 | 23.2 | |
2 | 20.2 | 20.4 | 23.4 | |
3 | 20.3 | 20.3 | 24.2 | |
4 | 20.5 | 20.6 | 23.6 | |
完成表格并依据该学生的实验数据计算,该实验中生成1水时放出的热量为
(结果保留一位小数)。
【考点】
中和热的测定;
能力提升
真题演练