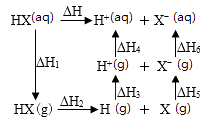1.
I.完成下列问题。
(1)①已知常温时红磷比白磷稳定,在下列反应中:
4P(白磷,s)+5O2(g)=2P2O5(s) ∆H1
4P(红磷,s)+5O2(g)=2P2O5(s) ∆H2
则有:∆H1∆H2(填“>”,“<”,“=”)。
②在25℃,101kPa下,无水乙醇的燃烧热∆H=-1366.8kJ/mol,则乙醇燃烧的热化学方程式为。
(2)常温常压下,氯气和水反应的能量变化关系如图所示。

请回答下列问题:
①该反应是(填“吸热”或“放热”)反应,原因是。
②)写出该反应的热化学方程式:(反应热用含E1、E2的代数式表示)。
II.甲醇的合成
(3)已知:CO(g)+O2(g)=CO2(g) ∆H1
H2(g)+O2(g)=H2O(g) ∆H2
CH3OH(g)+O2(g)=CO2(g)+2H2O(g) ∆H3
以CO(g)和H2(g)为原料合成甲醇的反应为CO(g)+2H2(g)=CH3OH(g)。该反应的∆H=(用含∆H1、∆H2、∆H3的式子表示)。
【考点】
盖斯定律及其应用;
基础巩固
能力提升
变式训练
拓展培优
真题演练