1.
某兴趣小组设计了利用MnO2和H2SO3生成MnS2O6 , 再与Na2CO3反应制备Na2S2O6∙2H2O的方案:

(1)
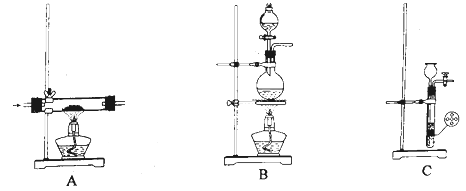
采用下图所示装置制备SO2 , 仪器a的名称为;写出实验室制SO2的化学方程式: 。
(2)
步骤Ⅱ应分数次加入MnO2 , 原因是。
(3)
步骤Ⅳ中滴入饱和Na2CO3溶液发生反应化学方程式:。
(4)
步骤Ⅲ滴加饱和Ba(OH)2溶液的目的是。
(5)
步骤Ⅳ生成MnCO3沉淀,判断Mn2+已沉淀完全的操作是。
(6)
将步骤Ⅴ中正确操作或现象的标号填入相应括号中。

![]()
A.蒸发皿中出现少量晶体
B.使用漏斗趁热过滤
C.利用蒸发皿余热使溶液蒸干
D.用玻璃棒不断搅拌
E.等待蒸发皿冷却
【考点】
常用仪器及其使用;
物质的分离与提纯;
能力提升
真题演练

 ;
; (未配平,部分生成物略)。
(未配平,部分生成物略)。




 步骤Ⅱ.产品中
步骤Ⅱ.产品中 
