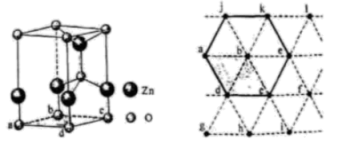
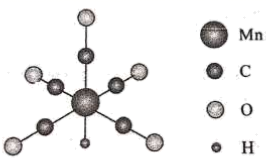
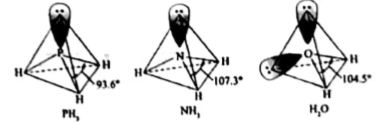
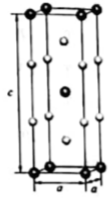
1.
HI是医药及农药的原料,关于HI的转化如下图:

已知:。请回答:
(1)
写出棕黄色溶液A中所有阴离子。
(2)
根据步骤③④,给出相关微粒与 结合能力由弱到强的顺序。
(3)
下列说法正确的是_______。
A.
步骤②需涉及到分液操作
B.
无色溶液F中不可能含有
结合能力由弱到强的顺序。
(3)
下列说法正确的是_______。
A.
步骤②需涉及到分液操作
B.
无色溶液F中不可能含有 C.
白色固体G是AgCl
D.
与
C.
白色固体G是AgCl
D.
与 的配位能力:
的配位能力: (4)
写出步骤①中化学反应的离子方程式。
(5)
设计实验检验溶液D中的金属阳离子。
(4)
写出步骤①中化学反应的离子方程式。
(5)
设计实验检验溶液D中的金属阳离子。
【考点】
配合物的成键情况;
能力提升
真题演练


 , 其中心原子杂化方式为:,其空间构型为;与其互为等电子体的一种阴离子是:。
, 其中心原子杂化方式为:,其空间构型为;与其互为等电子体的一种阴离子是:。
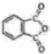 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺(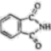 )都是合成菁的原料,后者熔点高于前者,主要原因是。
)都是合成菁的原料,后者熔点高于前者,主要原因是。