1.
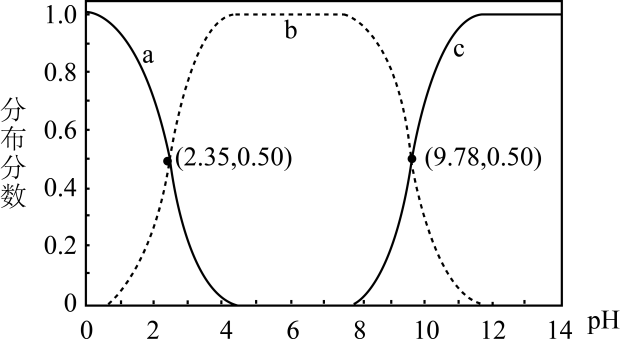
某温度下,Mg2+与不同pH的Na2CO3体系反应可生成不同的沉淀。下面图1表示Na2CO3体系中各含碳粒子的物质的量分数与pH的关系。图2表示Mg2+与不同pH的Na2CO3体系反应生成沉淀的情况,其中曲线Ⅰ的离子浓度关系符合c(Mg2+)·c2(OH-)=Ksp[Mg(OH)2];曲线Ⅱ的离子浓度关系符合c(Mg2+)·c(CO )=Ksp[MgCO3][注:起始c(Na2CO3)=0.1mol/L,不同pH下c(CO
)=Ksp[MgCO3][注:起始c(Na2CO3)=0.1mol/L,不同pH下c(CO )由图1得到]。
)由图1得到]。

下列说法正确的是
A.
上述Na2CO3体系呈中性时, 一定是10-3.25
B.
符合c(
一定是10-3.25
B.
符合c( )>c(
)>c( )>c(H2CO3)的pH范围:6.37<pH<10.25
C.
pH=9,c(Mg2+)=0.01mol/L时,溶液中只存在MgCO3沉淀
D.
pH=8,c(Mg2+)=0.1mol/L时可发生反应:Mg2++2
)>c(H2CO3)的pH范围:6.37<pH<10.25
C.
pH=9,c(Mg2+)=0.01mol/L时,溶液中只存在MgCO3沉淀
D.
pH=8,c(Mg2+)=0.1mol/L时可发生反应:Mg2++2 =Mg(OH)2↓+CO2↑
=Mg(OH)2↓+CO2↑
【考点】
离子浓度大小的比较;
基础巩固
能力提升
变式训练
拓展培优
真题演练