1.
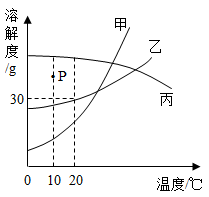
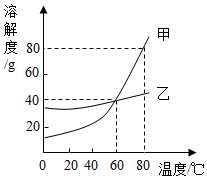
下图是甲、乙物质的溶解度曲线,下列说法正确的是

A.
甲的溶解度大于乙的溶解度
B.
t2℃时,甲、乙的溶液中溶质质量分数相等
C.
t3℃时,等质量的甲、乙的饱和溶液中甲溶液含水较多
D.
t3℃时,100g溶质质量分数为20%的甲溶液若变为饱和溶液,需加入20克甲
【考点】
固体溶解度曲线及其作用;
基础巩固
能力提升
变式训练
拓展培优
真题演练