1.
SO2是一种重要的化工原料,其性质的探究、废气处理及合理利用一直是科研人员研究的热点。回答下列问题:
(1)
Ⅰ.燃煤烟气中含有SO2 , 为了治理雾霾天气,工厂采用多种方法实现烟气脱硫。“湿式吸收法”是利用吸收剂与SO2发生反应从而脱硫。下列试剂不适合用作该法吸收剂的是____(填标号)。
A.
氨水
B.
CaCl2溶液
C.
Na2CO3溶液
D.
石灰乳
(2)
某化工厂用如图所示工艺流程除去燃煤产生的SO2。
(3)
Ⅱ.某化学兴趣小组同学为比较SO2与氯水的漂白性,设计了如图所示实验装置。
(4)
反应开始后,观察到B、D两个试管中的品红溶液均褪色,停止反应后,分别加热B、D两试管一段时间,B中现象为,D中现象为。
(5)
某同学将SO2和Cl2同时通入品红溶液中,发现溶液未褪色,其原因是(用化学方程式表示)。
(6)
装置C的作用是。
①该反应中的FeSO4作用是;
②标准状况下,当利用上述工艺流程除去11.2LSO2时,消耗O2的物质的量为mol。


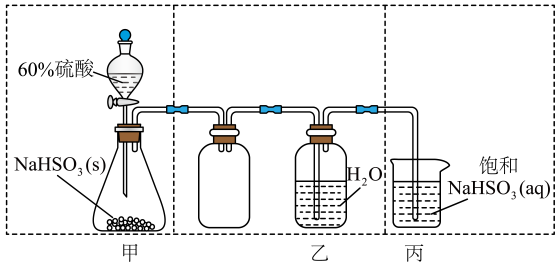
用装置A制备SO2气体,发生反应的化学方程式为。
【考点】
二氧化硫的性质;
性质实验方案的设计;
制备实验方案的设计;
能力提升
真题演练