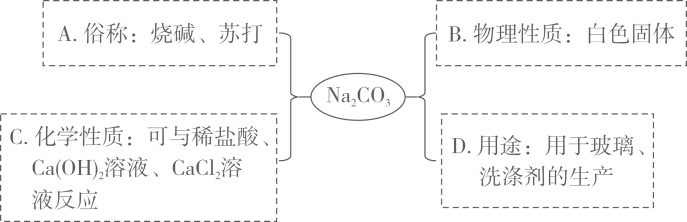
1.
小明同学向NaHCO3溶液中加入CaCl2溶液时观察到出现气泡和沉淀,这与认知产生冲突!继而展开探究,他将10%CaCl2溶液加至10mL不同浓度的NaHCO3溶液中,现象如表。已知:碳酸氢钙易溶于水:Ca2+与在溶液中无法大量共存,会生成微溶于水的硫酸钙沉淀。
实验编号 | 浓度 | 现象 |
I | 10% | 滴加1滴出现白色沉淀,有较多气泡产生 |
II | 5% | 滴加1滴出现白色沉淀,30s后有少量气泡产生 |
III | 1% | 滴加10滴出现浑浊 |
IV | 0.5% | 滴加52滴出现浑浊 |
【解释与推论】
(1)NaHCO3的俗称是________。
(2)根据实验I的实验现象,推测NaHCO3与CaCl2反应化学方程式:。
(3)为进一步确定实验IV中,反应后溶液溶质的成分进行猜想(不考虑气体溶解):
①NaCl ②NaCl、CaCl2 ③________。
可取少量反应后的溶液于试管中,加入足量的________(填字母)后观察现象,最终确定猜想②正确。
A.碳酸钠溶液 B.二氧化碳 C.硝酸银溶液 D.稀硫酸
【思考交流】
(4)小林将CaCl2溶液滴至NaHCO3溶液时却发现无沉淀,原因可能是________。
【考点】
常用盐的用途;
盐的化学性质;
基础巩固
能力提升
变式训练
拓展培优
真题演练