1.
某小组用W形管探究C还原 后的气体产物。
后的气体产物。
(1)
按照配比,混合相应质量的C粉和 粉末,并充分混合、研磨。
粉末,并充分混合、研磨。
(2)
实验探究1:
(3)
实验探究2:探究 与C反应能否生成
与C反应能否生成 (4)
进一步用仪器测量实验探究2产生的气体,得到以下图像:
(4)
进一步用仪器测量实验探究2产生的气体,得到以下图像:
编号 | 粉末① | 粉末② | 粉末③ |
C原子与O原子个数比 | |||
C粉质量 | |||
| x |
g。

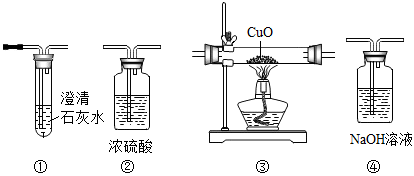
步骤1:如图a,称取研磨均匀后的粉末①装入A处,B处放入
澄清石灰水,用金属网罩住酒精灯加热。一段时间后,A处粉末变成红色,B处澄清石灰水变浑浊。请写B处出相关化学方程式。
步骤2:分别用粉末②、粉末③重复上述实验,一段时间后,均出现A处粉末变成红色,B处澄清石灰水变浑浊。
根据上述实验结果可以得出的实验探究1的结论是。

步骤1:如图形管
处放入
氧化铜粉末,凹槽
处不放置药品。点燃酒精灯,并对
处固体加热5分钟,无明显现象。
步骤2:另取W形管,取粉末①装入
处。从另一端放入
氧化铜粉末于
处,加热5分钟,发现
处
无明显变化。
步骤3:分别用粉末②、粉末③重复上述实验,加热5分钟,发现处
变成红色。
实验探究2中,步骤1的目的是。

①请问用粉末③进行实验时产生的气体对应曲线为。
②从定量角度分析,C还原生成
的含量增加的原因可能是。
【考点】
碳、一氧化碳、氢气还原氧化铜实验;
实验探究物质的组成成分以及含量;
能力提升
真题演练