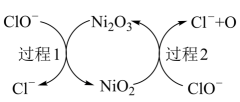
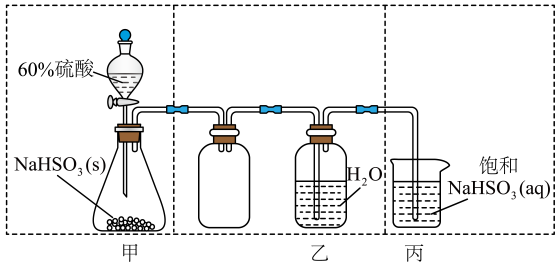
1.
标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH先增大后减小,当通入SO2112mL时,溶液pH最大,则原氢硫酸溶液的物质的量浓度为____mol·L-1。
A.
0.1
B.
0.05
C.
0.01
D.
0.005
【考点】
二氧化硫的性质;