1.
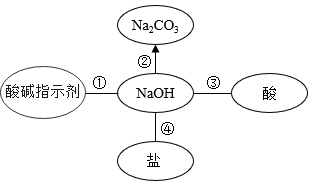
构建知识网络是一种重要的学习方法。下面是某同学整理的有关氢氧化钠的化学性质的知识网络,能相互反应的物质之间用短线“—”表示,通过一步反应能直接转化的两种物质之间用箭头“→”表示(从反应物指向生成物),请填写下列空格:
(1)
若①选用的酸碱指示剂为紫色石蕊试液,溶液颜色为色。
(2)
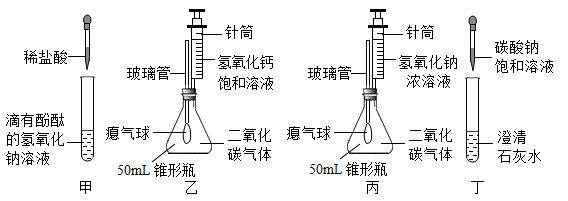
若②为碱与非金属氧化物反应,请写出转化②的化学方程式,可以用如图装置来进行该实验,实验现象为。
 (3)
反应③的实质为(从离子相互结合的角度分析)。
(4)
性质④,将氢氧化钠固体和某种硫酸盐混合研磨能散出有刺激性气味的气体。推测这种硫酸盐的化学式可能是。
(3)
反应③的实质为(从离子相互结合的角度分析)。
(4)
性质④,将氢氧化钠固体和某种硫酸盐混合研磨能散出有刺激性气味的气体。推测这种硫酸盐的化学式可能是。

【考点】
碱的化学性质;
能力提升
真题演练