1.
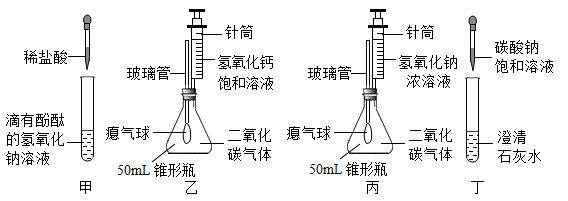
某兴趣学习小组在学习碱的化学性质时,进行了如图所示的实验:
(1)
写出甲实验中观察到的现象是:。
(2)
丙实验中滴加氢氧化钠溶液后,锥形瓶中气球的变化是。
(3)
丁实验中发生反应的化学方程式为。
(4)
同时向乙和丙装置中分别注入5mL氢氧化钙饱和溶液、5mL40%的氢氧化钠浓溶液(如图),乙和丙中观察到的不同现象有,产生这些不同现象的主要原因是。
【考点】
碱的化学性质;
能力提升
真题演练