1.
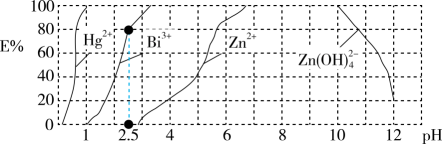
用双硫腺(H2Dz,二元弱酸)~CCl4络合萃取法可从工业废水中提取金属离子,从而达到污水处理的目的。如在分离污水中的Cu2+时,先发生络合反应:Cu2++2H2Dz Cu(HDz)2+2H+ , 再加入CCl4 , Cu(HDz)2就很容易被萃取到CCl4中。如图是用上述方法处理含有Hg2+、Bi3+、Zn2+的废水时的酸度曲线(E%表示金属离子以络合物形式被萃取分离的百分率),下列说法错误的是
Cu(HDz)2+2H+ , 再加入CCl4 , Cu(HDz)2就很容易被萃取到CCl4中。如图是用上述方法处理含有Hg2+、Bi3+、Zn2+的废水时的酸度曲线(E%表示金属离子以络合物形式被萃取分离的百分率),下列说法错误的是
A.
当分离过程中,Bi3+发生的络合反应为Bi3++3H2Dz Bi(HDz)3+3H+
B.
加NaOH溶液调节pH=11,一定存在关系:c(Na+)>c(D
Bi(HDz)3+3H+
B.
加NaOH溶液调节pH=11,一定存在关系:c(Na+)>c(D )=c[Zn(OH)
)=c[Zn(OH) ]>c(OH—)>c(H+)
C.
NaHDz溶液存在关系:c(D
]>c(OH—)>c(H+)
C.
NaHDz溶液存在关系:c(D )+c(OH-)=c(H2Dz)+c(H+)
D.
若pH=2.5且-lgc(H2Dz)=pH时,络合反应达到平衡,则H2Dz与Bi3+络合反应平衡常数约为5
)+c(OH-)=c(H2Dz)+c(H+)
D.
若pH=2.5且-lgc(H2Dz)=pH时,络合反应达到平衡,则H2Dz与Bi3+络合反应平衡常数约为5
【考点】
弱电解质在水溶液中的电离平衡;
离子浓度大小的比较;
能力提升
变式训练
拓展培优
真题演练



 。
。





