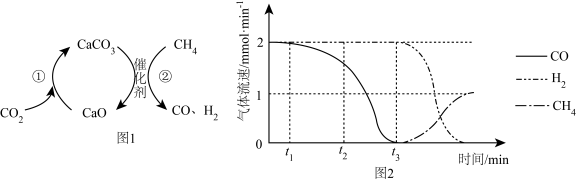
1.
某反应 的速率方程为
的速率方程为 , 其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为
, 其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为 。改变反应物浓度时,反应的瞬时速率如表所示:
。改变反应物浓度时,反应的瞬时速率如表所示:
0.25 | 0.050 | 1.4 |
0.50 | 0.050 | 2.8 |
1.00 | 0.050 | 5.6 |
0.50 | 0.100 | 2.8 |
下列说法正确的是( )
A.
速率方程中的 、
、 B.
该反应的速率常数
B.
该反应的速率常数 C.
增大反应物浓度,k增大导致反应的瞬时速率加快
D.
在过量的B存在时,反应掉87.5%的A所需的时间是375min
C.
增大反应物浓度,k增大导致反应的瞬时速率加快
D.
在过量的B存在时,反应掉87.5%的A所需的时间是375min
【考点】
化学反应速率;