1.
硫氧粉(Na2SO3)广泛应用于化工生产中,可用碳酸钠和二氧化硫反应制取。为探究某硫氧粉样品的成分,某化学兴趣小组的同学设计了如下实验。
【查阅资料】
①Na2SO3易溶于水,能与稀盐酸或稀硫酸发生反应生成SO2 , 能与氯化钡溶液反应生成白色沉淀。
②SO2能使品红溶液褪色,常用品红溶液检验SO2;能使澄清的石灰水变浑浊。
③CO2不能使品红溶液褪色,不能与酸性高锰酸钾溶液反应。
【探究一】硫氧粉样品的成分
【提出猜想】猜想1:Na2SO3 猜想2:Na2SO3、Na2CO3
【实验探究】
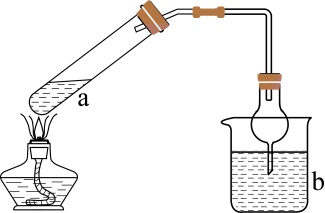
取少量硫氧粉样品,进行如下实验,选择所需装置对气体X的成分进行探究。

所需装置的连接顺序:气体X→(填字母序号)。B装置的作用是;若出现现象,证明气体X的成分为SO2 , 说明猜想1正确。
【探究二】该硫氧粉样品久置后的成分
【提出猜想】猜想1:Na2SO3 猜想2:。 猜想3:Na2SO4
【实验探究】
取少量久置的硫氧粉样品加水溶解,请设计实验方案验证猜想2成立:。
【反思交流】久置硫氧粉变质的原因(用化学方程式表示)。
【考点】
物质检验实验方案的设计;
化学实验方案的评价;
能力提升
变式训练
拓展培优
真题演练