1.
邻苯二甲酰亚胺( )是一种重要的亚胺,是
)是一种重要的亚胺,是 合成法制备胺的原料。某实验室模拟氨水法以邻苯二甲酸酐为原料制备
合成法制备胺的原料。某实验室模拟氨水法以邻苯二甲酸酐为原料制备 。
。
反应原理:
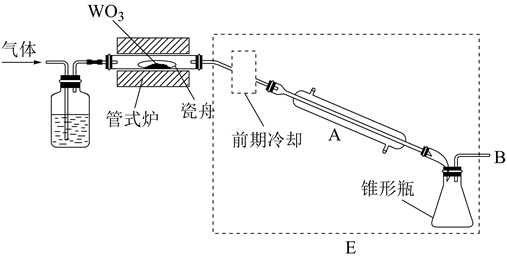
实验装置如图:
相关物质的物理性质如表:
物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 |
邻苯二甲酸酐 | 148 | 131~134 | 284 | 不溶于冷水,微溶于热水,稍溶于乙醇 |
邻苯二甲酰亚胺 | 147 | 232~235 | 366 | 微溶于热水,易溶于乙醇,易溶于碱溶液 |
实验步骤:
I.向三颈烧瓶中加入
邻苯二甲酸酐,边搅拌边滴入
浓氨水(稍过量),加热至
, 待固体完全溶解后停止加热。将三颈烧瓶右端口所连装置取下改为蒸馏装置,继续加热,将溶液中的水及过量的氨蒸馏回收,此时烧瓶中有白色固体析出。
II.继续升温至 , 固体熔化,反应60分钟后,停止加热。冷却至室温,热水洗涤固体、抽滤、烘干,得到粗品白色粉末
。
III.向白色粉末中加入适量乙醇,加热回流使固体恰好溶解,___________,将滤液降温冷却,有白色晶体析出,抽滤、洗涤、烘干后得白色晶体。
请回答下列问题:
(1)
仪器A的名称为,其中装的试剂为。
(2)
步骤II所得粗品中的杂质主要为。
(3)
步骤III的目的是利用重结晶进一步提纯邻苯二甲酰亚胺,该步骤中划线部分应补全的操作是。选择乙醇作为提纯溶剂的主要原因是。
(4)
本实验中邻苯二甲酰亚胺的产率最接近于。(填标号)
(5)
邻苯二甲酰亚胺还可以用由邻二甲苯( )与氨气、氧气在加热条件下催化反应一步制得,写出该反应的化学方程式:。
)与氨气、氧气在加热条件下催化反应一步制得,写出该反应的化学方程式:。
a.85% b.80% c.75% d.70%
 )与氨气、氧气在加热条件下催化反应一步制得,写出该反应的化学方程式:。
)与氨气、氧气在加热条件下催化反应一步制得,写出该反应的化学方程式:。
【考点】
物质的分离与提纯;
制备实验方案的设计;
化学实验方案的评价;
能力提升
真题演练