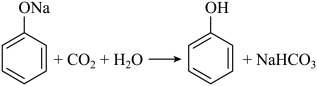
1.
Ⅰ.写出下列反应的离子方程式:
(1)鸡蛋壳(主要成分为碳酸钙)溶解在醋酸中:。
(2) 溶液与
溶液与 溶液混合:。
溶液混合:。
(3)AlCl3加入氨水产生白色沉淀:。
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其中可能含有中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2mL该溶液用溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(4)原溶液中一定存在的离子是,一定不存在的离子是。
(5)按上述实验操作,(填“能”或“不能”)确定原溶液中有 , 若不能请说明原因:。
, 若不能请说明原因:。
【考点】
离子方程式的书写;