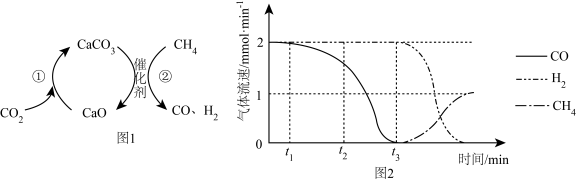
1.
某探究性学习小组利用 溶液和酸性
溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下(不考虑溶液混合所引起的体积缩小)。
溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下(不考虑溶液混合所引起的体积缩小)。
实验序号 | 试验温度 |
|
| 溶液颜色褪至无色时所需时间 | |||
A | 293 | 2 | 0.02 | 5 | 0.1 | 5 | |
B | 2 | 0.02 | 4 | 0.1 | 8 | ||
C | 313 | 2 | 0.02 | 0.1 | 6 | ||
(1)
写出该反应的离子方程式(已知:草酸是弱酸,产物有 、
、 等);每消耗
等);每消耗 , 则反应中转移
, 则反应中转移 电子。
(2)
通过实验
电子。
(2)
通过实验 、
、 可探究(填外部因素)的改变对反应速率的影响,其中
可探究(填外部因素)的改变对反应速率的影响,其中 ;通过实验可探究温度变化对化学反应速率的影响。
(3)
若
;通过实验可探究温度变化对化学反应速率的影响。
(3)
若 , 则由此实验可以得出的结论是;利用实验
, 则由此实验可以得出的结论是;利用实验 中数据计算,用
中数据计算,用 的浓度变化表示的反应速率为(用含有
的浓度变化表示的反应速率为(用含有 的式子表示)。
(4)
同学们在实验中发现反应速率总是如图所示,其中
的式子表示)。
(4)
同学们在实验中发现反应速率总是如图所示,其中 时间内速率变快的主要原因可能是:①产物(
时间内速率变快的主要原因可能是:①产物( 或
或 )是反应的催化剂:②。
)是反应的催化剂:②。

【考点】
化学反应速率;
化学反应速率的影响因素;
能力提升
真题演练