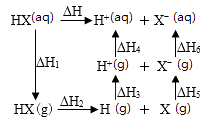1.
NH3是一种重要的化工产品,可用于生产尿素[CO(NH2)2]、处理烟气等。
(1)
工业上合成尿素的反应:2NH3(g)+CO2(g)═CO(NH2)2(l)+H2O(g) △H。
(2)
某实验小组为了模拟工业上合成尿素,在恒温恒容的真空密闭容器中充入一定量的CO2和NH3发生反应:2NH3(g)+CO2(g)═CO(NH2)2(l)+H2O(g),反应过程中混合气体中NH3的体积分数如图所示。
已知合成尿素的反应分两步进行:
2NH3(g)+CO2(g)═NH2COONH4(s) △H1
NH2COONH4(s)═CO(NH2)2(l)+H2O(g) ΔH2
其能量变化曲线如图所示,则△H、△H1和△H2由小到大的顺序为。


①A点的逆反应速率v逆(CO2)B点的正反应速率v正(CO2)(填“>”“<”或“=”)。
②对于有气体参与的反应,平衡常数Kp可用气体组分(B)的平衡分压p(B)代替该气体的物质的量浓度c(B)。实验测得体系平衡时的压强为10MPa,列式计算该反应的平衡常数Kp=MPa-2(提示:写出Kp的表达式再代入数据进行计算,分压=总压×体积分数)。
③L(L1、L2),x可分别代表压强或温度。如图表示L一定时,该反应CO2(g)的平衡转化率随x的变化关系。

x代表的物理量为,判断L1、L2的大小关系,并简述理由:。
【考点】
反应热的大小比较;