1.
学习完测定空气中氧气的含量后,同学们对课本实验进行了改进:
(已知:白磷和红磷都能在空气中燃烧生成五氧化二磷)

(1)
如图1,红磷在瓶中燃烧产生大量,燃烧停止并冷却至室温后打开弹簧夹,可以观察到水倒流入集气瓶约占空气体积的 , 写出该反应的文字表达式。通过该实验现象,还能判断出剩余气体的物理性质是溶于水。
(2)
图2装置中,打开止水夹之前,气球的大小变化是。
(3)
图3装置中,若白磷量不足,活塞最终停在刻度线______(填序号)。
A.
4处
B.
5处
C.
, 写出该反应的文字表达式。通过该实验现象,还能判断出剩余气体的物理性质是溶于水。
(2)
图2装置中,打开止水夹之前,气球的大小变化是。
(3)
图3装置中,若白磷量不足,活塞最终停在刻度线______(填序号)。
A.
4处
B.
5处
C.
 之间
D.
之间
D.
 之间
(4)
图4装置中,集气瓶中空气的体积为
之间
(4)
图4装置中,集气瓶中空气的体积为 , 若装置漏气,测定结果会(填“偏大”或“偏小”或“无影响”)。改进后,实验结束时流入集气瓶的水的体积为
, 若装置漏气,测定结果会(填“偏大”或“偏小”或“无影响”)。改进后,实验结束时流入集气瓶的水的体积为 , 则测得的空气中氧气的体积分数为。
(5)
利用图二中的传感器可以实时监测实验过程中装置内的压强、温度和氧气浓度,得到3条曲线,变化趋势如图6所示。
, 则测得的空气中氧气的体积分数为。
(5)
利用图二中的传感器可以实时监测实验过程中装置内的压强、温度和氧气浓度,得到3条曲线,变化趋势如图6所示。

X曲线表示(选填“温度”或“氧气浓度”)变化趋势。压强曲线中,段气压变化的原因是。
【考点】
测定空气中的氧气含量;
能力提升
真题演练









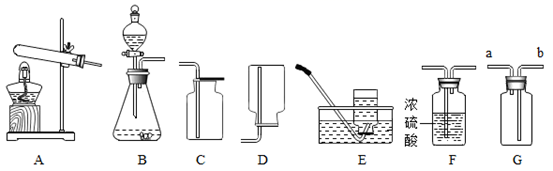

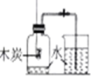 测定空气中氧气的含量
测定空气中氧气的含量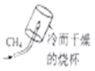 探究甲烷中是否含碳元素
探究甲烷中是否含碳元素 验证质量守恒定律
验证质量守恒定律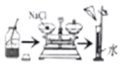 配制一定溶质质量分数的氯化钠溶液
配制一定溶质质量分数的氯化钠溶液