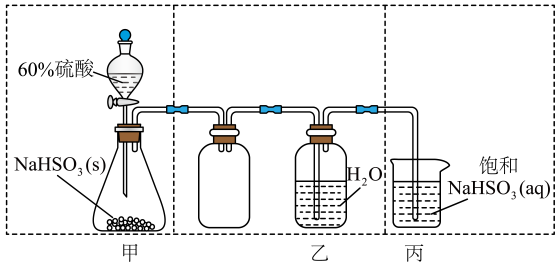
1.
实验室制备次硫酸氢钠甲醛( )的步骤如下:向烧瓶中的亚硫酸钠溶液通入
)的步骤如下:向烧瓶中的亚硫酸钠溶液通入 制得
制得 。将装置A中导气管换成橡皮塞,再加入锌粉和甲醛溶液,在80~90℃下,反应约3h,冷却至室温,抽滤,将滤液置于真空蒸发仪蒸发浓缩,冷却结晶。下列说法错误的是
。将装置A中导气管换成橡皮塞,再加入锌粉和甲醛溶液,在80~90℃下,反应约3h,冷却至室温,抽滤,将滤液置于真空蒸发仪蒸发浓缩,冷却结晶。下列说法错误的是

A.
可用亚硫酸钠固体和70%硫酸来制取二氧化硫气体
B.
多孔球泡的作用是增大气体与溶液的接触面积,使反应充分进行
C.
装置B中试剂可以是NaOH溶液
D.
装置A最好采用油浴或沙浴加热
【考点】
二氧化硫的性质;
基础巩固
能力提升
变式训练
拓展培优
真题演练