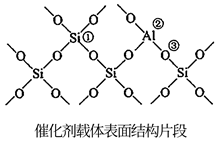
1.
回答下列问题:
(1)
合成氨反应的能量变化如图所示,
(2)
室温下, (Si为-4价)是一种无色气体,遇到空气能发生爆炸性自燃,生成
(Si为-4价)是一种无色气体,遇到空气能发生爆炸性自燃,生成 固体和
固体和 。已知室温下
。已知室温下 自燃时每转移0.05mol电子,放出a kJ的热量,该反应的热化学方程式为。
(3)
如图是
自燃时每转移0.05mol电子,放出a kJ的热量,该反应的热化学方程式为。
(3)
如图是 和
和 反应生成1mol
反应生成1mol  过程中的能量变化示意图,表格中若已知下列数据:
过程中的能量变化示意图,表格中若已知下列数据:
(4)
电化学合成氨有望解决哈伯法的不足,以NO为氮源通过电解法制取氨气成为研究热点之一、已知酸性溶液中反应时,该过程存在(a)、(b)两种反应历程且均通过五步完成,示意如下:

该反应的热化学方程式是: ΔH=。
化学键 | H-H | |
键能/ | 435 | 943 |
计算N-H的键能为。


这两种途径的焓变分别为ΔH(a),ΔH(b),两者的关系是(填“大于”“等于”“小于”)。
【考点】
反应热和焓变;
盖斯定律及其应用;
能力提升
真题演练







 (g) ∆H1<0
(g) ∆H1<0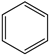 (g)+15O2(g)⇌12CO2(g)+6H2O(l) ∆H4
(g)+15O2(g)⇌12CO2(g)+6H2O(l) ∆H4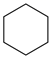 (g)+9O2(g)=6CO2(g)+6H2O(l) ∆H5
(g)+9O2(g)=6CO2(g)+6H2O(l) ∆H5